#biotecnología
Text
O elixir da juventude está dentro de nós....
Telômeros são as "pontas" dos cromossomos que protegem o material genético e modulam a longevidade das células.
Há tempos, os alquimistas acreditavam na existência de um elixir da juventude, que supostamente se encontrava no chamado ouro potável, cujas propriedades permitiriam a cura e a regeneração do organismo, prolongando a vida. Na alquimia, o ouro era considerado um metal puro e perfeito, associado ao sol e à imortalidade.
Acredita-se que o ouro potável, por ser uma forma mais refinada e purificada de ouro, poderia transmitir essas propriedades aos humanos, proporcionando-lhes juventude eterna.
Nessa mesma linha de pensamento, alguns filósofos antigos acreditavam em um suposto elixir da longa vida, também conhecido como a água dos filósofos, que traria longevidade aos seus consumidores. Na Bíblia, inclusive, o precioso elixir foi referido como "a água da vida".
Mas histórias a parte, o fato é que nunca ninguém conseguiu produzir até o momento um elixir da longa vida, talvez porque o segredo dessa longevidade esteja muito perto. Dentro de nós!
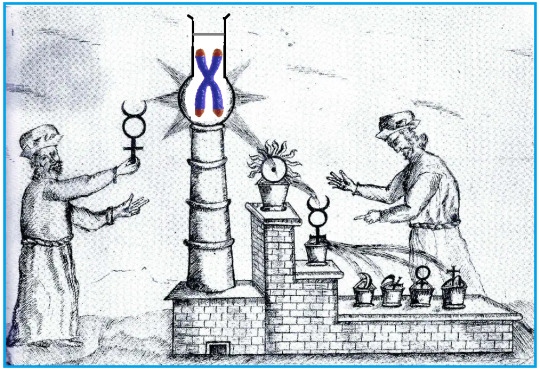
Os telômeros são formados por sequências repetitivas de bases nitrogenadas de DNA (TTAGGG) localizadas nas extremidades dos cromossomos. Essas sequências repetitivas de nucleotídeos atuam como "capas protetoras" do material genético localizado no restante do cromossomo, desempenhando papel importante na estabilidade e segurança dos genes durante a divisão celular (mitose), assim como na "regulação" da longevidade das células.
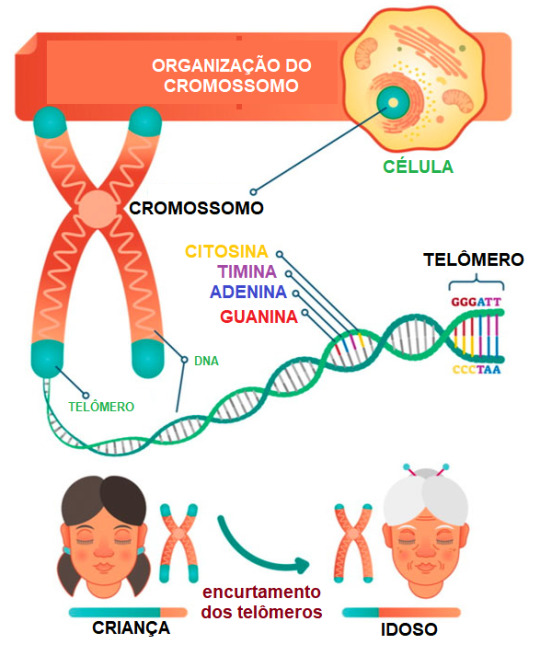
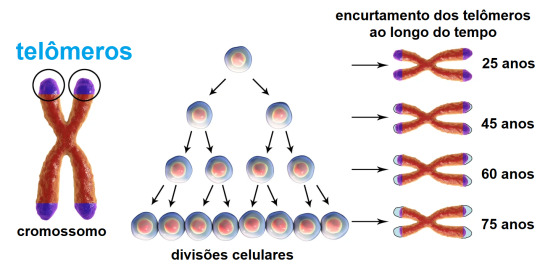
À medida que as células se replicam por mitose ao longo do tempo, os telômeros tendem a encurtar gradualmente. Isso ocorre porque antes da mitose, mais precisamente na fase S da intérfase , a DNA polimerase (enzima responsável pela replicação do DNA), não consegue completar a replicação até o final do cromossomo. Como resultado, as extremidades dos cromossomos são gradualmente perdidas a cada ciclo celular (são perdidos de 50 a 100 nucleotídeos a cada divisão celular).
Quando os telômeros se tornam muito curtos, as células podem entrar em senescência (um estado de parada do crescimento) ou sofrer apoptose (morte celular programada). Estudos científicos demonstraram que o encurtamento dos telômeros está relacionado ao envelhecimento e ao desenvolvimento de doenças associadas à idade.
As células-tronco e certas células do sistema imunológico, no entanto, são dotadas de telomerase, uma enzima que pode "regenerar" os telômeros mantendo a integridade dos cromossomos nessas células. A telomerase adiciona sequências repetitivas de DNA às extremidades dos cromossomos, compensando o encurtamento natural que ocorre durante a replicação do DNA.
A atividade da telomerase é geralmente alta em células-tronco embrionárias, permitindo que elas permaneçam com telômeros longos. Assim, as células-tronco embrionárias preservam a capacidade de se dividirem e se diferenciarem em diferentes tipos de células. Já as células-tronco adultas e principalmente as células permanentes diferenciadas apresentam níveis menores de telomerase quando comparadas às células´ embrionárias.
Diversos estudos científicos demonstraram que o encurtamento dos telômeros ao longo do tempo está também indiretamente relacionado ao desenvolvimento de algumas doenças, entre elas:
Doenças cardiovasculares: o encurtamento dos telômeros tem sido associado a um maior risco de doenças cardiovasculares, como doença arterial coronariana, hipertensão arterial e acidente vascular cerebral.
Câncer: telômeros mais curtos estão frequentemente presentes em células cancerígenas. O encurtamento dos telômeros pode levar a instabilidade genômica, o que favorece a ocorrência de mutações que contribuem para o desenvolvimento do câncer.
Doenças pulmonares: pacientes com doenças pulmonares crônicas, como fibrose pulmonar idiopática e doença pulmonar obstrutiva crônica (DPOC), geralmente apresentam telômeros mais curtos em suas células pulmonares.
Doenças neurodegenerativas: há evidências sugerindo que o encurtamento dos telômeros pode estar envolvido em doenças neurodegenerativas, como doença de Alzheimer, doença de Parkinson e esclerose lateral amiotrófica (ELA).
Síndromes genéticas: certas síndromes (raras) estão associadas ao encurtamento dos telômeros, tais a Síndrome de Werner, a Síndrome de disqueratose congênita e a Síndrome de Bloom.
Recentemente, pesquisadores da USP verificaram que animais com carência da enzima telomerase nas células-tronco da medula óssea geram número insuficiente de células de defesa (leucócitos), ou geram células de defesa menos eficazes, além de problemas no fígado. Linhas de pesquisa em outras universidades espalhadas nos Estados Unidos e Europa apontam que a diminuição da atividade da telomerase nas células-tronco da medula óssea pode ter consequências negativas, tais como:
Envelhecimento do sistema hematopoiético: com o encurtamento dos telômeros nas células-tronco da medula óssea ao longo do tempo, as capacidades de autorrenovação e de diferenciação em células sanguíneas diminuem. Isso pode contribuir para o envelhecimento do sistema hematopoiético e para o desenvolvimento de doenças relacionadas à idade, como a anemia.
Aumento do risco de doenças hematológicas: a diminuição da telomerase nas células-tronco da medula óssea pode estar associada a um maior risco de desenvolvimento de certas doenças hematológicas, como a Síndrome Mielodisplásica (SMD) e a leucemia mieloide aguda (LMA).
Disfunção imunológica: a diminuição da atividade da telomerase pode afetar a capacidade das células-tronco da medula óssea de produzir células do sistema imunológico (leucócitos). Isso pode resultar em uma diminuição da resposta imunológica eficiente e em aumento da suscetibilidade a infecções e doenças relacionadas ao sistema imunológico.
No entanto, é importante ressaltar que a relação causal direta entre a diminuição da telomerase nas células-tronco da medula óssea e o desenvolvimento de doenças ainda precisa ser completamente esclarecida.
Pesquisadores da University College de Londres, no Reino Unido, liderados pelo Dr. Alessio Lanna, acenaram com um método preventivo promissor contra o envelhecimento do sistema imunológico. Esses cientistas descobriram que no combate a determinados agentes invasores, determinadas células do sistema imunológico (macrófagos e células dendríticas) podem "transferir telômeros" para os chamados linfócitos T (células de defesa fundamentais) por meio de vesículas membranosas extracelulares. Essa transferência resulta em aumento do comprimento de determinados telômeros dos linfócitos T em até 30 vezes mais que a ação da enzima telomerase.
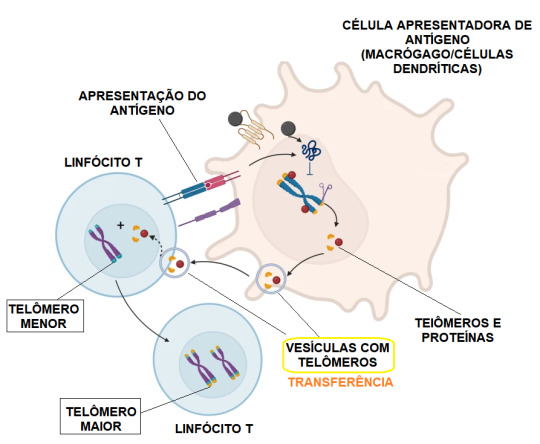
Após a incrível descoberta, a equipe da University College passou a investigar e a purificar as vesículas carregadas de telômeros. A ideia é tentar adicioná-las aos linfócitos T para aumentar a longevidade dessas células em estado natural, independentemente da ocorrência de uma infecção. No decorrer da pesquisa, os cientistas concluíram que as vesículas membranosas carregadas de telômeros poderiam ser administradas com sucesso, por exemplo, quando combinadas com uma vacina, de modo a prolongar a duração da resposta imunológica do imunizante.
Mas será que, em tese, seria possível aplicar para fins preventivos ou regenerativos a enzima telomerase nas células de algum paciente?
Bem, sim!
Mas o fato é que ainda não há relatos de ensaios clínicos que utilizaram essa abordagem, afinal mexer com telomerase e telômeros não é tão simples assim!
A aplicação da telomerase como uma abordagem terapêutica ainda é uma área de pesquisa em andamento. É verdade que teoricamente a aplicação ou a ativação da enzima telomerase poderia prolongar a vida útil das células e retardar o encurtamento dos telômeros, reduzindo os efeitos do envelhecimento e prevenindo certas doenças associadas ao encurtamento dos telômeros.
Só que a utilização indiscriminada da telomerase poderia também resultar em efeitos negativos à saúde, pois sabe-se que algumas células cancerígenas são capazes de ativar mecanismos que preservam os telômeros, permitindo que continuem se dividindo indefinidamente. Esses mecanismos incluem a ativação da enzima telomerase. Nesse caso, adicionar telomerase extra poderia significar "apagar o fogo com gasolina", isto é, estimular a atividade da telomerase em células normais também poderia aumentar o risco do desenvolvimento de tumores.
No entanto, a pesquisa sobre a manipulação da telomerase e da extensão dos telômeros continua em andamento, e várias abordagens estão sendo exploradas para o desenvolvimento de tratamentos potenciais.
Tudo é recente! A descoberta dos telômeros e a relação deles com o envelhecimento ocorreu na década de 1970. Os cientistas Elizabeth Blackburn, Carol Greider e Jack Szostak foram premiados com o Prêmio Nobel de Fisiologia ou Medicina em 2009 pela descoberta da telomerase e do papel dos telômeros na proteção do material genético. Desde então, muitas pesquisas estão sendo financiadas para entender melhor a função dos telômeros e da telomerase.
Embora ainda haja muito a aprender sobre telômeros e telomerase, avanços na tecnologia permitirão melhor entendimento sobre os impactos desses elementos à saúde humana.
O que acontecerá nas relações humanas, o dia em que a ciência mostrar formas seguras e eficazes das células preservarem seus telômeros? Envelheceríamos de forma mais lenta? Nesse caso, o sonho dos alquimistas seria alcançado? O que viria depois?
Leia também:
1-https://jornal.usp.br/ciencias/cientistas-descobrem-efeitos-importantes-da-doenca-dos-telomeros-no-sistema-imunologico/ (acesso em 06 de julho de 2023)
2-https://www.scielo.br/j/rbhh/a/rrjrCBxN8KFgtKh8FmccNwG/?lang=pt (acesso em 06 de julho de 2023)
3-https://oglobo.globo.com/saude/medicina/noticia/2022/09/longevidade-descoberto-mecanismo-que-retarda-envelhecimento-do-sistema-imunologico-mostra-estudo-da-nature.ghtml (acesso em 06 de julho de 2023)
4-https://genotipia.com/genetica_medica_news/transferencia-de-telomeros/ (acesso em 06 de julho de 2023)
5-https://www.ucl.ac.uk/news/2022/sep/new-mechanism-extends-life-immune-system?_ga=2.107367938.1640029816.1688673765-1213671299.1688673765 (acesso em 06 de julho de 2023)
6-https://sentcell.life/about/ (acesso em 06 de julho de 2023)
7-https://www.nature.com/articles/s41423-022-00949-z (acesso em 06 de julho de 2023)
8-https://www.ucl.ac.uk/news/2022/sep/new-mechanism-extends-life-immune-system (06 de julho de 2023)
5 notes
·
View notes
Text
• 12 de Dezembro de 2022
Citogenética. Surto.


#livros#study blog#stemblr#studywithme#study motivation#stem student#study aesthetic#study#science#citogenética#biotechnology#biotecnología
5 notes
·
View notes
Text
La biotecnología.
La biotecnología agrícola ha transformado radicalmente las prácticas agrícolas y las relaciones sociales de producción a nivel global. La manipulación genética de cultivos, como la soja, ha creado semillas que no pueden reutilizarse, introduciendo mecanismos genéticos que provocan su infertilidad tras un año. Este avance tecnológico, que permite crear semillas más resistentes, también ha generado una mayor dependencia de la tecnología y un mercado altamente concentrado.
Impacto Ambiental y Biodiversidad
Los cultivos transgénicos, como la soja, han sido asociados con un incremento en el uso de herbicidas y otros agrotóxicos, lo que conlleva consecuencias negativas para el medio ambiente y la salud humana. Además, promueven un modelo de agricultura altamente industrializado que contribuye a la expansión de la frontera agrícola en zonas naturales, poniendo en peligro la biodiversidad y alterando ecosistemas.
Dependencia Tecnológica y Económica
La brecha entre países desarrollados y en desarrollo se amplía debido a la dependencia tecnológica que generan las nuevas técnicas de mejoramiento de cultivos. Las semillas transgénicas, al ser patentadas por grandes empresas, crean una situación de dependencia económica para los agricultores, quienes deben adquirir nuevas semillas cada temporada junto con los agroquímicos necesarios.
Problemas Éticos y Sociales
La liberación de transgénicos al medio ambiente plantea problemas éticos y sociales imprevisibles. La contaminación genética de cultivos convencionales o ecológicos y plantas silvestres emparentadas es una preocupación creciente, ya que la repercusión de estos nuevos organismos en la naturaleza es totalmente imprevisible.
Desafíos para la Agricultura Sostenible
Frente a estos desafíos, surgen movimientos sociales y propuestas teóricas que buscan replantear la relación entre la sociedad y la naturaleza. Se aboga por un modelo de desarrollo sostenible que reconozca los límites ecológicos del planeta y promueva una relación más armónica y respetuosa con el entorno natural.
Conclusión
La revolución biogenética, a través de la manipulación genética de cultivos, ha traído una serie de implicaciones que van más allá de la mejora en la resistencia de las semillas. La dependencia tecnológica y económica, el impacto ambiental y los dilemas éticos y sociales son aspectos que deben ser considerados críticamente. Es esencial trabajar hacia prácticas agrícolas que sean sostenibles y equitativas, garantizando la seguridad alimentaria y la protección del medio ambiente para las generaciones futuras.

View On WordPress
1 note
·
View note
Text
Estudio del Cedla afirma que sustitución de importaciones de diésel con biocombustibles no será tan significativa como lo proyectado por el Gobierno
Un estudio realizado por el Centro de Estudios para el Desarrollo Laboral y Agrario (Cedla) ha revelado que la implementación del proyecto de biodiésel en Bolivia no logrará reducir las importaciones de diésel en un 43%, como lo había proyectado el Gobierno, sino que solo se reducirán en un 5% en 2024 y un 10% en 2025. Además, el investigador del Cedla Carlos Arze advirtió sobre los altos costos…
View On WordPress
#aceite de palma africana#aceite de soya#Ahorro#Alcohol#alternativa ecológica#Armin Dorgathen#biocombustibles#Biodiésel#Biotecnología#Carlos Arze#Cedla#comunicado de prensa#condiciones técnicas#costos ambientales#costos económicos#Diésel#diésel renovable#El Alto#Estado#estatutos#Estudio#etanol#Exportación#Gobierno#Importación#importaciones#Industria Boliviana de Aceites Ecológicos#ingresos.#instalación#Instituto Nacional de Innovación Agropecuaria y Forestal
0 notes
Text
José Mª Aznar reclama que se regule la IA y la biotecnología para evitar un “riesgo existencial” para el ser humano
El expresidente del Gobierno José María Aznar ha reclamado regulación internacional para la Inteligencia Artificial (IA) y la biotecnología con el objetivo de evitar un “riesgo existencial” para el ser humano y que las personas no sean sustituidas por las máquinas.
Así se ha pronunciado este martes el presidente de FAES, durante su ponencia en el ciclo de Conferencias Circulares del Cámara…

View On WordPress
0 notes
Text
DRAFT Design Web: Impulsando el Progreso y la Innovación en Navarra
En un mundo cada vez más digitalizado, la innovación y el progreso se han convertido en pilares fundamentales para el desarrollo de cualquier región. En este contexto, Navarra ha demostrado un firme compromiso con el avance tecnológico y la mejora de la c
En un mundo cada vez más digitalizado, la innovación y el progreso se han convertido en pilares fundamentales para el desarrollo de cualquier región. En este contexto, Navarra ha demostrado un firme compromiso con el avance tecnológico y la mejora de la calidad de vida de sus habitantes. Y en el corazón de esta apuesta por la innovación se encuentra DRAFT Design Web, la empresa liderada por el…

View On WordPress
#Activos Digitales#Agricultura#Biotecnología#Calidad de Vida#Ciberseguridad#Competitividad#Comunicación Digital#Crecimiento Económico#Desarrollo Empresarial#Desarrollo Local#Desarrollo Sostenible#Desarrollo Tecnológico#Digitalización#Draft Design Web#Economía#Eficiencia#Emprendimiento#Empresas Navarras#estrategia digital#Futuro Tecnológico#Gobierno de Navarra#Industria Alimentaria#Innovación#Innovación Empresarial#Innovación en Biotecnología#Innovación en Ciberseguridad#Innovación en IA#Innovación en Salud#inteligencia artificial#Investigación y Desarrollo
0 notes
Text
Productores demandan al Gobierno agilizar autorizaciones para el uso de biotecnología en la producción de granos
Golpeados por los efectos del cambio climático y el contrabando, productores de agricultura del país exigen al Gobierno agilizar autorizaciones para el uso de biotecnología en la producción de granos. El gerente de Anapo, Jaime Hernández, explicó la relación de esta producción con el maíz, trigo, girasol y sorgo. El vicepresidente de Anapo, Richard Paz, explicó que los productores necesitan…

View On WordPress
#Agrícolas#Anapo#Biotecnología#Cambio Climático#Contrabando#Producción#Santa Cruz#Soya HB4#Trigo HB4
0 notes
Text
ROCHE presenta su Reporte de Sostenibilidad 2022
Programas y alianzas público-privadas para el desarrollo mejoran la atención de pacientes panameños
Este año, por primera vez en Panamá, la compañía Roche presentó su Reporte de Sostenibilidad 2022, el cual muestra resultados que impactan a la población en sus diferentes áreas: social, económica y ambiental.
A nivel regional, más de 40 iniciativas durante 2022 reflejan el compromiso de…

View On WordPress
0 notes
Text
Científicos regeneran los nervios de dedos con una bioimpresora 3D
BIOIMPRESIONES. Científicos japoneses regeneraron con éxito los nervios periféricos de las manos de tres pacientes con el uso de una bioimpresora 3D.
El Hospital de la Universidad de Kioto informó que el uso de dichas tecnologías permitió la regeneración y mejora en la vida de tres pacientes.
Según la agencia Jiji Press, los investigadores usaron una bioimpresora 3D de la empresa Cyfuse…

View On WordPress
0 notes
Text
MUJERES EN BIOTECNOLOGÍA: INNOVANDO EN CICY.

El TECNM campus CRODE Mérida les invita a participar en la videoconferencia "Mujeres en Biotecnología: Innovando en CICY", la cual será impartida por la Dra. María Marcela Gamboa Angulo, Profesora-Investigadora adscrita a la unidad de Biotecnología del Centro de Investigación Científica de Yucatán. Regístrate. IMPORTANTE: El link de acceso a la reunión se brinda al final del registro, no olvides copiarlo y guardarlo.
0 notes
Text
Se lanzó 500 becas formativas para que jóvenes tengan su primer empleo digital
Se lanzó 500 becas formativas para que jóvenes tengan su primer empleo digital
Se lanzó 500 becas formativas para jóvenes denominado “Hacia mi Primer Empleo Digital” y busca favorecer la competitividad de los recursos humanos en el desarrollo de capacidades y competencias acordes al nuevo paradigma de la economía basado en el conocimiento.
Podrán acceder estudiantes de 16 a 25 años, de los últimos años de la Educación Secundaria Orientada, tecnicaturas superiores o…

View On WordPress
#beca#Big Data Jujuy Summit#Biotecnología#Carlos Sadir#CEO#Desarrollador Full Stack#Desarrollador Web Full Stack#Desarrollo Web#DH#Digital House#Digital House para América Latina#economía del conocimiento#EdTech#Eduardo Bruchou#electromovilidad#energías renovables#Gerardo Morales#Hacia mi Primer Empleo Digital#Hidrógeno Verde#IES#Institutos de Educación Superior#Juan Carlos Abud#María Teresa Bovi#Tecnicaturas Superiores
0 notes
Text
Crean ratones con dos padres gracias a células madre: ¿Podría esto aplicarse a humanos en el futuro?
Científicos han creado ratones bebés con dos padres por primera vez convirtiendo células madre de ratón macho en células femeninas en un laboratorio. Si bien esto plantea la posibilidad lejana de hacer lo mismo en humanos, los expertos advierten que solo nacieron muy pocos embriones de ratón y nadie sabe si la misma técnica funcionaría en células madre humanas.

No obstante, “es una estrategia muy ingeniosa que se ha desarrollado para convertir células madre masculinas en células madre femeninas”, dijo Diana Laird, experta en células madre y reproducción de la Universidad de California, San Francisco, que no participó en la investigación. “Es un paso importante tanto en la biología de células madre como en la reproducción”.
Los científicos describen su trabajo en un estudio publicado en la revista Nature. Primero, tomaron células de la piel de las colas de ratones machos y las transformaron en “células madre pluripotentes inducidas”, que pueden desarrollarse en muchos tipos diferentes de células o tejidos. Luego, a través de un proceso que implicó su cultivo y tratamiento con un fármaco, convirtieron las células madre de ratón macho en células femeninas y produjeron óvulos funcionales. Finalmente, fertilizaron esos óvulos e implantaron los embriones en ratones hembras. Alrededor del 1% de los embriones - 7 de 630 - se convirtieron en crías de ratón vivas. Los ratones parecían crecer normalmente y podían reproducirse de manera normal.
En un comentario publicado junto al estudio de Nature, Laird y su colega Jonathan Bayerl, dijeron que el trabajo “abre nuevas vías en la biología de la reproducción y la fertilidad” para animales y personas. En el futuro, por ejemplo, podría ser posible reproducir mamíferos en peligro de extinción a partir de un solo macho. “Incluso podría proporcionar una plantilla para permitir que más personas”, como parejas del mismo sexo masculinas, “tengan hijos biológicos, evitando los problemas éticos y legales de los óvulos de donantes”, escribieron.
Pero también plantearon varias precauciones. ¿La más notable? La técnica es extremadamente ineficiente. Dijeron que no está claro por qué solo una pequeña fracción de los embriones colocados en ratones gestantes sobrevivieron; las razones podrían ser técnicas o biológicas. También destacaron que aún es demasiado pronto para saber si el protocolo funcionaría en células madre humanas. Laird también dijo que los científicos deben ser conscientes de las mutaciones y errores que pueden introducirse en una placa de cultivo antes de usar células madre para hacer óvulos.
El estudio es el último en probar nuevas formas de crear embriones de ratón en el laboratorio. El verano pasado, científicos de California e Israel crearon embriones de ratón "sintéticos" a partir de células madre sin esperma del padre, óvulo de la madre o útero. Esos embriones imitaron a los embriones de ratón naturales hasta 8 ½ días después de la fertilización, conteniendo las mismas estructuras, incluyendo una como un corazón latiente. Los científicos dijeron que el logro podría sentar las bases para crear embriones humanos sintéticos para la investigación en el futuro.
Referencia:
Murakami, K., Hamazaki, N., Hamada, N. et al. Generation of functional oocytes from male mice in vitro. Nature (2023). https://doi.org/10.1038/s41586-023-05834-x
0 notes
Text
Homo Deus: Breve historia del mañana
Tras el éxito de Sapiens, Yuval Noah Harari vuelve su mirada al futuro para ver hacia dónde nos dirigimos.
Bestseller del New York Times con 1 millón de ejemplares vendidos
Yuval Noah Harari, autor de Sapiens, un fenómeno internacional unánimemente aclamado por la crítica, regresa con una secuela igualmente original, convincente y provocadora, centrando su atención en el futuro de la humanidad…

View On WordPress
#8499928080#9788499928081#Biotecnología#Breve historia del mañana#DEBATE#Homo Deus#Ingeniería bioquímica#Inteligencia artificial y machine learning#Libros Guadarrama#Yuval Noah Harari
0 notes
Text
La biotecnología ha tenido un impacto significativo en la producción de alimentos y la agricultura en las últimas décadas. Esta rama de la ciencia utiliza técnicas moleculares y celulares para desarrollar productos y procesos que pueden mejorar la calidad y cantidad de los cultivos y alimentos. Una de las formas en que la biotecnología ha…
0 notes
Photo
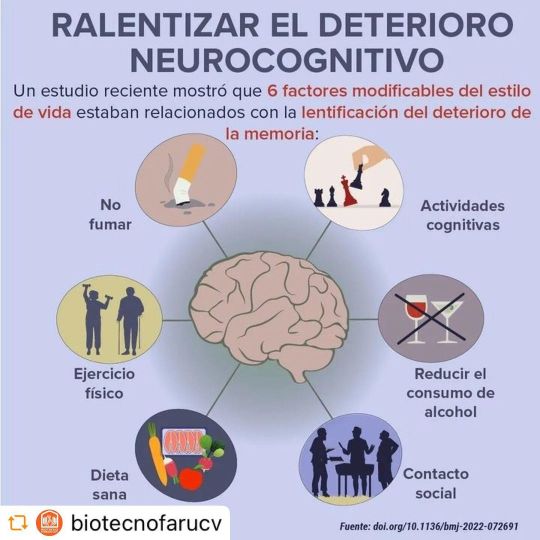
#RG @biotecnofarucv Ralentización del deterioro neurocognitivo Se prevé que de aquí a 2050 aumentará al doble el número de personas de 60 años o más. Es comprensible que la preocupación por prevenir o mitigar los problemas de salud asociados al envejecimiento suscite un gran interés. Recientemente, en varios estudios se han identificado factores relacionados con el estilo de vida y enfoques clínicos que pueden frenar el deterioro de la memoria. Los resultados de un amplio estudio poblacional indicaron que seis comportamientos saludables lentificaban el deterioro cognitivo, independientemente de la expresión de ApoE4. Tras ajustar los factores socioeconómicos y de salud, los investigadores descubrieron que los estilos de vida favorables se asociaban a un deterioro de la memoria más lento que el promedio en el curso de una década. Una dieta sana tuvo el mayor efecto, seguida de la actividad cognitiva y el ejercicio físico. Los participantes con un estilo de vida favorable o promedio tenían respectivamente casi 90% y 30% menos de probabilidades de padecer demencia o deterioro cognitivo leve, en comparación con los que tenían un estilo de vida desfavorable. Otro estudio reciente ha mostrado que incluso las sesiones cortas de ejercicio pueden ayudar a proteger contra el deterioro cognitivo. En un pequeño estudio de adultos sanos, 6 minutos de ciclismo de alta intensidad aumentaron los niveles circulantes de factor neurotrófico derivado del cerebro (BDNF), una proteína clave implicada en la memoria, la neuroplasticidad y el aprendizaje, más que periodos más largos de ciclismo ligero o ayuno. Fuente: https://espanol.medscape.com/verarticulo/5910414; @medscape Por favor Síguenos y realiza nuestros cursos en: @biosaber.pcr @diplomadocalidadmicrob @biotecnofarucv @menciondemicrobiologiaaplicada #saludybienestar #cognitivo #enfermedaddealzheimer #salud #microbiología #microbiologia #biotecnología #biotecnologia #bioanalistas #ciencia #science #farmacia #bioquimica #bioquímica #genética #genetica #laboratorio #animallovers #crueltyfree #biologia #biología #quimicofarmacéutico #virtual #online #cursos #diplomado #felizsabado #felizsábado https://www.instagram.com/p/ComBUspO-hQ/?igshid=NGJjMDIxMWI=
#rg#saludybienestar#cognitivo#enfermedaddealzheimer#salud#microbiología#microbiologia#biotecnología#biotecnologia#bioanalistas#ciencia#science#farmacia#bioquimica#bioquímica#genética#genetica#laboratorio#animallovers#crueltyfree#biologia#biología#quimicofarmacéutico#virtual#online#cursos#diplomado#felizsabado#felizsábado
1 note
·
View note