#lecanemab
Link
“The first drug to slow the destruction of the brain in Alzheimer's has been heralded as momentous.
The research breakthrough ends decades of failure and shows a new era of drugs to treat Alzheimer's - the most common form of dementia - is possible.
Yet the medicine, lecanemab, has only a small effect and its impact on people's daily lives is debated.
And the drug works in the early stages of the disease, so most would miss out without a revolution in spotting it.
Lecanemab attacks the sticky gunge - called beta amyloid - that builds up in the brains of people with Alzheimer's.
For a medical field littered with duds, despair and disappointment, some see these trial results as a triumphant turning point.
Alzheimer's Research UK said the findings were "momentous.”
One of the world's leading researchers behind the whole idea of targeting amyloid 30 years ago, Prof John Hardy, said it was "historic" and was optimistic "we're seeing the beginning of Alzheimer's therapies." Prof Tara Spires-Jones, from the University of Edinburgh, said the results were "a big deal because we've had a 100% failure rate for a long time..."
The large-scale trial involved 1,795 volunteers with early stage Alzheimer's. Infusions of lecanemab were given every fortnight.
The results, presented at the Clinical Trials on Alzheimer's Disease conference in San Francisco and published in the New England Journal of Medicine, are not a miracle cure. The disease continued to rob people of their brain power, but that decline was slowed by around a quarter over the course of the 18 months of treatment.
The data is already being assessed by regulators in the US who will soon decide whether lecanemab can be approved for wider use. The developers - the pharmaceutical companies Eisai and Biogen - plan to begin the approval process in other countries next year.” -via BBC, via Future Crunch, 12/1/22
47 notes
·
View notes
Text
Therapien für Alzheimer: Was erwartet uns?
Trotz vieler vielversprechender Fortschritte bei der Behandlung der Alzheimer-Krankheit kommen neue Therapien nur langsam in Gang.
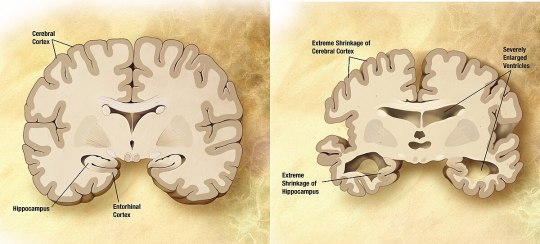
Vergleich eines gesunden Gehirns und eines Gehirns mit fortgeschrittenen Alzheimer-Schäden
Die derzeitigen Alzheimer-Therapien verbessern vorübergehend die Symptome des Gedächtnisverlusts und der Probleme beim Denken und Schlussfolgern.
Diese Alzheimer-Behandlungen steigern die Leistung von Chemikalien im Gehirn, die Informationen von einer Gehirnzelle zur anderen übertragen. Dazu gehören Cholinesterasehemmer und das Medikament Memantin. Diese Behandlungen können jedoch den zugrunde liegenden Verfall und das Absterben von Gehirnzellen nicht aufhalten. Je mehr Zellen absterben, desto weiter schreitet die Alzheimer-Krankheit fort.
Die Experten sind vorsichtig, aber hoffnungsvoll, was die Entwicklung von Behandlungen angeht, die das Fortschreiten der Alzheimer-Krankheit aufhalten oder verzögern können. Die Wissenschaft versteht immer besser, wie die Krankheit das Gehirn verändert. Dies hat zur Erforschung potenzieller Alzheimer-Behandlungen geführt, die den Krankheitsprozess beeinflussen können.
Künftige Alzheimer-Behandlungen könnten eine Kombination von Medikamenten umfassen. Dies ist vergleichbar mit der Behandlung vieler Krebsarten oder von HIV/AIDS, bei denen mehr als ein Medikament eingesetzt wird.
Die derzeitigen Alzheimer-Therapien verbessern vorübergehend die Symptome des Gedächtnisverlusts und der Probleme beim Denken und Schlussfolgern.
Diese Alzheimer-Behandlungen steigern die Leistung von Chemikalien im Gehirn, die Informationen von einer Gehirnzelle zur anderen übertragen. Dazu gehören Cholinesterasehemmer und das Medikament Memantin (Namenda). Diese Behandlungen können jedoch den zugrunde liegenden Verfall und das Absterben von Gehirnzellen nicht aufhalten. Je mehr Zellen absterben, desto weiter schreitet die Alzheimer-Krankheit fort.
Die Experten sind vorsichtig, aber hoffnungsvoll, was die Entwicklung von Behandlungen angeht, die das Fortschreiten der Alzheimer-Krankheit aufhalten oder verzögern können. Die Experten verstehen immer besser, wie die Krankheit das Gehirn verändert. Dies hat zur Erforschung potenzieller Alzheimer-Behandlungen geführt, die den Krankheitsprozess beeinflussen können.
Künftige Alzheimer-Behandlungen könnten eine Kombination von Medikamenten umfassen. Dies ist vergleichbar mit der Behandlung vieler Krebsarten oder von HIV/AIDS, bei denen mehr als ein Medikament eingesetzt wird.
Hier einige der Strategien, die derzeit untersucht werden.
Die Plaques ins Visier nehmen
Einige der neuen Alzheimer-Behandlungen zielen auf Verklumpungen des Proteins Beta-Amyloid, die so genannten Plaques, im Gehirn ab. Plaques sind ein charakteristisches Anzeichen der Alzheimer-Krankheit.
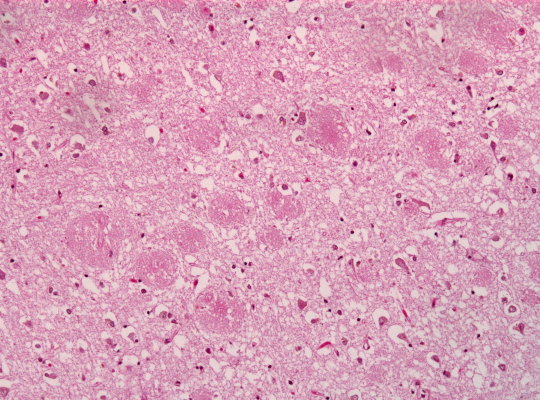
Amyloid-Plaques im Hirngebwebe
Zu den Strategien, die auf Beta-Amyloid abzielen, gehören:
Aktivierung des Immunsystems
Als monoklonale Antikörper bekannte Medikamente können verhindern, dass Beta-Amyloid zu Plaques verklumpt. Sie können auch bereits gebildete Beta-Amyloid-Plaques entfernen. Dazu helfen sie dem Körper, sie aus dem Gehirn zu entfernen. Diese Medikamente ahmen die Antikörper nach, die Ihr Körper natürlicherweise als Teil der Reaktion Ihres Immunsystems auf fremde Eindringlinge oder Impfstoffe produziert.
Im Juni 2021 hat die US-amerikanische Food and Drug Association (FDA) den monoklonalen Antikörper Aducanumab (Aduhelm) für die Behandlung der Alzheimer-Krankheit bei einigen Menschen zugelassen. Das Arzneimittel wurde bei Menschen mit früher Alzheimer-Krankheit, einschließlich Menschen mit leichter kognitiver Beeinträchtigung aufgrund der Alzheimer-Krankheit, untersucht.
Das Medikament wurde in den Vereinigten Staaten zugelassen, weil es die Beta-Amyloid-Plaques entfernt. Aber es wird nicht häufig eingesetzt. Die Studien über seine Wirksamkeit bei der Verlangsamung des kognitiven Verfalls sind uneinheitlich. Auch der Versicherungsschutz ist begrenzt.
Ein weiteres Alzheimer-Medikament, Lecanemab (Leqembi), hat sich als vielversprechend für Menschen mit leichter Alzheimer-Krankheit und leichter kognitiver Beeinträchtigung aufgrund der Alzheimer-Krankheit erwiesen. Die FDA hat das Medikament im Jahr 2023 zugelassen. Das Medikament wird über eine Infusion in den Arm verabreicht.
Eine klinische Studie der Phase 3 ergab, dass Lecanemab den kognitiven Abbau bei Menschen mit früher Alzheimer-Krankheit um 27 % verlangsamt. Das Medikament wirkt, indem es Beta-Amyloid-Plaques im Gehirn entfernt. Diese Studie war die bisher größte, in der untersucht wurde, ob die Entfernung von Beta-Amyloid-Plaques aus dem Gehirn den Krankheitsverlauf verlangsamen kann.
In einer weiteren laufenden Studie wird untersucht, wie wirksam Lecanemab bei Menschen mit einem Alzheimer-Risiko sein kann. Dazu gehören Menschen, die einen Verwandten ersten Grades, z. B. einen Elternteil oder ein Geschwisterkind, mit der Krankheit haben.
Donanemab, ein weiterer monoklonaler Antikörper, hat sich ebenfalls als vielversprechend erwiesen. Das Medikament wurde in eine Phase-3-Studie aufgenommen. Ergebnisse werden im Jahr 2023 erwartet.
Der monoklonale Antikörper Solanezumab zeigte jedoch keine Vorteile für Personen mit präklinischer, leichter oder mittelschwerer Alzheimer-Krankheit. Solanezumab senkte das Beta-Amyloid im Gehirn nicht, was der Grund dafür sein könnte, dass es nicht wirksam war.
Synapsen schützen
Ein ursprünglich als mögliches Krebsmittel entwickeltes Medikament - Saracatinib - wird nun bei der Alzheimer-Krankheit getestet.
Bei Mäusen schaltete Saracatinib ein bestimmtes Protein aus, wodurch die Synapsen wieder zu funktionieren begannen. Synapsen sind die winzigen Zwischenräume zwischen Gehirnzellen, über die die Zellen miteinander kommunizieren. Bei den Tieren in der Studie konnte ein gewisser Gedächtnisverlust rückgängig gemacht werden. Derzeit laufen Versuche mit Saracatinib als möglicher Alzheimer-Behandlung am Menschen.
Beta-Amyloid-Produktion verringern
Diese Therapien können die Menge des im Gehirn gebildeten Beta-Amyloids verringern. Die Forschung hat gezeigt, dass Beta-Amyloid in zwei Schritten, die von verschiedenen Enzymen ausgeführt werden, aus einem "Mutterprotein" gebildet wird.
Mehrere experimentelle Arzneimittel zielen darauf ab, die Aktivität dieser Enzyme zu blockieren. Sie sind als Beta- und Gamma-Sekretase-Inhibitoren bekannt. Jüngste Studien haben gezeigt, dass die Beta-Sekretase-Hemmer den kognitiven Verfall nicht verlangsamen. Außerdem waren sie mit erheblichen Nebenwirkungen bei Menschen mit leichter oder mittelschwerer Alzheimer-Krankheit verbunden. Dies hat den Enthusiasmus für diese Medikamente verringert.
Verklumpungen des Tau-Proteins verhindern
Ein lebenswichtiges Transportsystem der Gehirnzellen bricht zusammen, wenn sich ein Protein namens Tau in winzige Fasern verdreht. Diese Fasern werden Tangles genannt. Sie sind eine weitere häufige Veränderung in den Gehirnen von Menschen mit Alzheimer. Forscher suchen nach einer Möglichkeit, die Bildung von Tangles durch Tau zu verhindern.
Tau-Aggregationshemmer und Tau-Impfstoffe werden derzeit in klinischen Studien untersucht.
Entzündungen hemmen
Die Alzheimer-Krankheit verursacht eine chronische, schwache Entzündung der Gehirnzellen. Die Forscher untersuchen Möglichkeiten zur Behandlung der Prozesse, die bei der Alzheimer-Krankheit zu Entzündungen führen. Das Medikament Sargramostim (Leukine) befindet sich derzeit in der Forschung. Das Medikament könnte das Immunsystem dazu anregen, das Gehirn vor schädlichen Proteinen zu schützen.
Erforschung der Insulinresistenz
In Studien wird untersucht, wie Insulin das Gehirn und die Funktion der Gehirnzellen beeinflussen kann. Forscher untersuchen, wie Insulinveränderungen im Gehirn mit der Alzheimer-Krankheit zusammenhängen könnten. Bei einem Versuch mit einem Insulin-Nasenspray wurde jedoch festgestellt, dass das Medikament das Fortschreiten der Alzheimer-Krankheit nicht verlangsamen kann.
Erforschung der Verbindung zwischen Herz und Kopf
Es gibt immer mehr Hinweise darauf, dass die Gesundheit des Gehirns eng mit der Gesundheit von Herz und Blutgefäßen zusammenhängt. Das Risiko, an Demenz zu erkranken, scheint sich bei vielen Erkrankungen, die das Herz oder die Arterien schädigen, zu erhöhen. Dazu gehören Bluthochdruck, Herzerkrankungen, Schlaganfall, Diabetes und ein hoher Cholesterinspiegel.
In einer Reihe von Studien wird untersucht, wie man diesen Zusammenhang am besten ausbauen kann. Zu den untersuchten Strategien gehören:
Gängige Medikamente gegen Risikofaktoren für Herzkrankheiten. Forscher untersuchen, ob Blutdruckmedikamente Menschen mit Alzheimer helfen können. Sie untersuchen auch, ob die Medikamente das Demenzrisiko verringern können.
Medikamente für neue Ziele. In anderen Studien wird genauer untersucht, wie der Zusammenhang zwischen Herzerkrankungen und Alzheimer auf molekularer Ebene funktioniert. Ziel ist es, neue potenzielle Arzneimittel für Alzheimer zu finden.
Änderung des Lebensstils. Forschungsergebnisse deuten darauf hin, dass Lebensstilmaßnahmen, die bekanntermaßen für das Herz vorteilhaft sind, dazu beitragen können, der Alzheimer-Krankheit vorzubeugen oder ihren Ausbruch zu verzögern. Zu diesen Lebensstilentscheidungen gehören Sport und eine herzgesunde Ernährung.
Hormone
In den 1990er Jahren deuteten Studien darauf hin, dass die Einnahme einer Hormonersatztherapie während der Perimenopause und der Menopause das Risiko einer Alzheimer-Erkrankung senkt. Die weitere Forschung ist jedoch uneinheitlich. In einigen Studien wurde kein kognitiver Nutzen einer Hormonersatztherapie festgestellt. Weitere Forschungen und ein besseres Verständnis der Beziehung zwischen Östrogen und kognitiven Funktionen sind erforderlich.
Beschleunigung der Forschung
Die Entwicklung neuer Medikamente ist ein langsamer Prozess. Das Tempo kann für Menschen mit Alzheimer und ihre Familien, die auf neue Behandlungsmöglichkeiten warten, frustrierend sein.
Um die Forschung zu beschleunigen, hat das Konsortium Critical Path for Alzheimer's Disease (CPAD) in den USA eine Partnerschaft gegründet, um Daten aus klinischen Alzheimer-Studien auszutauschen. Zu den CPAD-Partnern gehören Pharmaunternehmen, gemeinnützige Stiftungen und Regierungsberater. CPAD hieß früher Coalition Against Major Diseases (Koalition gegen schwere Krankheiten).
CPAD hat auch mit dem Clinical Data Interchange Standards Consortium zusammengearbeitet, um Datenstandards zu entwickeln. Die Forscher sind der Ansicht, dass Datenstandards und die gemeinsame Nutzung der Daten von Tausenden von Studienteilnehmern die Entwicklung wirksamerer Therapien beschleunigen werden.
#Alzheimer#Demenz#Forschung#Alzheimer-Krankheit#Memantin#Aducanumab#Lecanemab#CPAD#TAU-Protein#Beta-Amyloid#Amyloid-Plaques
2 notes
·
View notes
Link
Dr. Andrew Budson is Chief of Cognitive Behavioral Neurology at the VA Boston Healthcare System, Associate Director of the Boston University Alzheimer’s Disease Research Center, Professor of Neurology at Boston University, and Lecturer in Neurology at Harvard Medical School. He has written 9 books, including Six Steps to Managing Alzheimer’s Disease and Dementia, Why We Forget and How to Remember Better, and his latest, Seven Steps to Managing Your Aging Memory—now in its 2nd edition—which explains how to distinguish changes in memory due to Alzheimer's versus normal aging, what medications, diets, and exercise regimes can help, and the best habits, strategies, and memory aids to keep your memory strong. Sponsor: www.SeniorCareAuthority.com
0 notes
Text
NHS not ready for new Alzheimer's drugs lecanemab and donanemab, warns charity | BBC
Any new drug will always be welcomed, but as with any drug they have to be tested, costs assessed and more before any decision to proceed to use can be taken.
Yes, there will be side effects, but there are to any drug and it depends if the benefits outweigh the side effects and to what degree that has to be assessed, who is more likely to have side effects and what dosages are to be for most…
View On WordPress
0 notes
Text
Treatment postcode lottery
Tomorrow heralds an exciting day in psychiatry. In The Netherlands, donanemab clinical trial results will be published for the first time. We anticipate that they will be positive as a similar drug trial was published last year, for the trial drug lecanemab, that slowed down the cognitive decline in early Alzheimer’s disease that now has approval from the US food and drug…

View On WordPress
#alzheimers#alzheimers disease#cognitive impairment#cohesion#dementia#donanemab#fulfilment#insomnia#lecanemab#mental health#mental illness#old age#psychiatrist#sleep
0 notes
Text
Diagnóstico precoz en la enfermedad de Alzheimer
#DiagnósticoPrecoz en la enfermedad de #Alzheimer. Una colaboración de Luis Fernández
@luisfdezdguez
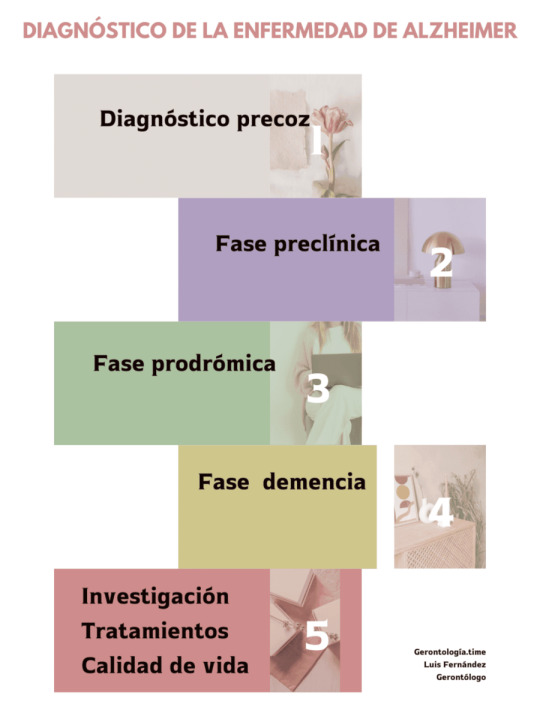
Diagnóstico precoz en la enfermedad de Alzheimer
El diagnóstico precoz en la enfermedad de Alzheimer es crucial para proporcionar un tratamiento efectivo y mejorar la calidad de vida. Permite planificar los cuidados, ofrecer apoyo emocional, promover la investigación, acceder a ensayos clínicos y abordar los problemas sociosanitarios.
La enfermedad de Alzheimer (EA) es la forma más común de…
View On WordPress
#Diagnosticar Alzheimer#Diagnóstico Precoz#Etapas del Alzheimer#Fases de las Demencias#Gerontología#Lecanemab#Luis Fernández - Gerontólogo#SEN#Sociedad Española de Neurología
0 notes
Text
New FDA-approved drug may revolutionize Alzheimer's treatment - Study Finds
1 note
·
View note
Text
According to the World Health Organisation (WHO), 10 million new instances of dementia are identified each year, making dementia and Alzheimer's one of the most prevalent diseases today. Dementia is the fifth biggest cause of mortality among all illnesses, affecting more than 55 million people globally.
After years of looking for a cure, a new medication is now presenting a ray of hope. Lecanemab has been demonstrated in clinical studies to delay the disease's related cognitive loss. The medication targets the brain's protein clumps, which many believe to be the disease's root cause.

#brain#alzheimer#demenia#aging#stroke#braincancer#brain 2023#brain conference#braindisorder#brain injury#neuroscience#drugs#nicotine#Lecanemab
1 note
·
View note
Text
Alzheimer's drug, FDA approved a new one
Alzheimer’s drug, FDA approved a new one
The U.S. Food and Drug Administration on Friday approved a second Alzheimer’s drug, lecanemab, despite reports of rare brain bleeds linked to use of the drug in some patients.
About Alzheimer’s drug, lecanemab
Alzheimer’s drug, lecanemab, is a monoclonal antibody. It is not a cure but works by binding to amyloid beta, a breakthrough for Alzheimer’s disease. In late November 2022, results from a…

View On WordPress
0 notes
Text
New year, new drug to treat Alzheimer's approved by FDA
New year, new drug to treat Alzheimer’s approved by FDA
This week, the U.S. Food and Drug Administration approved a new drug to treat those in the early stages of Alzheimer’s disease. The approval of lecanemab was welcomed by the Alzheimer’s Association, who urged the Centers for Medicare & Medicaid Services to cover the cost for its members. Some members of the medical community have a more guarded view of this latest Alzheimer’s treatment,…

View On WordPress
0 notes
Text
Wie ein schwedisches Start-up die Suche nach einem Alzheimer-Medikament neu beleben konnte
Vor einem Jahrzehnt gab ein großer Teil der Big Pharma eine der grausamsten Krankheiten der Menschheit auf. Doch dann erwies sich eine neue Behandlung als vielversprechend.
Gunilla Osswald spricht leise, als sie ihre letzten Tage bei AstraZeneca beschreibt. Nachdem sie 28 Jahre lang versucht hatte, Behandlungen für Patienten mit Hirnleistungsstörungen zu entwickeln, wurde ihr 2012 die traurige Aufgabe übertragen, einen großen schwedischen Forschungs- und Entwicklungsstandort zu schließen und 1300 Mitarbeiter zu entlassen.

Gunilla Oswald, Gründerin von BioArctic
Vor einem Jahrzehnt kürzte der schwedisch-britische Arzneimittelhersteller seine Investitionen in die Neurowissenschaften. Er war nicht der einzige. GSK, Pfizer und Bristol Myers Squibb gehörten zu den anderen großen Pharmaunternehmen, die die Suche nach Behandlungsmöglichkeiten für eine der rätselhaftesten Krankheiten der Menschheit einstellten. Damals galt die Alzheimer-Forschung als teuer und hoffnungslos. Die Investoren zogen es vor, dass die Unternehmen größeren Gewinnaussichten in Bereichen wie Krebs nachjagten.
Bei einem Blick über einen Konferenztisch in Stockholm räumt Osswald ein, dass die Neurowissenschaften für Arzneimittelhersteller riskant sind. "Es ist ein schwieriges Gebiet. Aber der Nutzen kann enorm sein, wenn man etwas erfolgreiches hat", sagt sie.
Nachdem AstraZeneca seinen Standort geschlossen hatte, gab Osswald nicht auf. Stattdessen übernahm sie die Leitung eines Start-up-Unternehmens mit nur 20 Mitarbeitern, das sich der Bekämpfung der Alzheimer-Krankheit widmete, und holte weitere Mitarbeiter von AstraZeneca hinzu. Ihr Ziel war es, ein Medikament zu entwickeln, das als erstes das Fortschreiten der Krankheit deutlich verlangsamen würde.
In dieser Hinsicht haben sie Fortschritte gemacht. In dieser Woche wird die US-amerikanische Arzneimittelbehörde Food and Drug Administration darüber entscheiden, ob der erste kommerziell verfügbare Arzneimittelkandidat von BioArctic, Lecanemab, der gemeinsam mit dem japanischen Arzneimittelhersteller Eisai und dem US-amerikanischen Biotech-Unternehmen Biogen entwickelt wurde, vollständig zugelassen wird.
Die FDA hat bereits im Januar eine Notfallzulassung erteilt, die auf Daten basierte, die zeigten, dass Lecanemab die Geschwindigkeit des kognitiven Abbaus bei Alzheimer-Patienten im Frühstadium um 27 Prozent verlangsamt - ein moderates, aber statistisch signifikantes Ergebnis. Mit der endgültigen Zulassung dürfte sich die Zahl der Patienten, die in den kommenden Monaten Zugang zu dem Medikament erhalten, erheblich erhöhen; es ist das erste Mal, dass Alzheimer-Patienten etwas einnehmen können, um das Fortschreiten ihrer Krankheit zu verlangsamen.
"Das ist wirklich ein großer Schritt nach vorn", sagt Osswald und erklärt, dass die bisherigen Medikamente nur einige Symptome lindern, nicht aber die Ursachen der Krankheit bekämpfen konnten.
Nicht alle sind damit einverstanden. Einige Forscher und Kliniker sind besorgt, dass die in der Studie beobachtete Verringerung des kognitiven Abbaus nicht "klinisch bedeutsam" ist, da viele Patienten keine große Wirkung spüren würden.
Sie befürchten, dass der Nutzen die Risiken nicht aufwiegt: Die Studie hat gezeigt, dass das Medikament zu Schwellungen und Blutungen im Gehirn führen kann. Die Patienten müssen bei der ersten Einnahme des Medikaments, das intravenös verabreicht wird, sorgfältig überwacht werden. Seit dem Ende der Studie mit 1795 Patienten sind mindestens drei Alzheimer-Patienten nach der Einnahme von Lecanemab an Hirnblutungen gestorben, darunter zwei Personen, die auch blutverdünnende Medikamente einnahmen. Eisai erklärte, das Medikament könne nicht direkt mit den Todesfällen in Verbindung gebracht werden.
Weltweit leiden etwa 55 Millionen Menschen an Demenz, davon bis zu 70 Prozent an Alzheimer - einer Krankheit, die Erinnerungen und die Fähigkeit zu kommunizieren und unabhängig zu leben auslöscht. In Deutschland schätzt die DZNE, dass die Krankheit den Staat bereits 83 Milliarden Euro pro Jahr kostet - das entspricht mehr als zwei Prozent des Bruttoinlandsprodukts. Die Krankheit ist belastend für die Patienten und ihre Familien und teuer für die überlasteten Gesundheitssysteme in Ländern mit einer alternden Bevölkerung.
Osswald wägt ihre Worte sorgfältig ab und hütet sich davor, verzweifelten Patienten zu große Versprechungen zu machen. "Es ist keine Heilung. Aber es kann ihnen hoffentlich zu einer längeren Zeit verhelfen, in der sie einigermaßen gesund sind", sagt sie.
Lecanemab ist nicht das einzige neue Alzheimermedikament mit Potenzial. Auf die Ergebnisse von BioArctic im letzten Herbst folgten rasch die Ergebnisse einer anderen vielversprechenden Studie für ein Medikament, Donanemab, von Eli Lilly.
Wenn beide Medikamente zugelassen werden, könnten sie letztendlich Kosten im Gesundheitswesen einsparen, da die Menschen länger gesund bleiben. Aber sie werden enorme Vorleistungen erfordern. Lecanemab wird in den USA offiziell 26.500 Dollar pro Jahr kosten, doch werden die Versicherer Rabatte aushandeln, die das Medikament billiger machen. Medicare, die von der US-Regierung unterstützte Versicherung für Senioren, hat zugesagt, für das Medikament zu zahlen, wenn es zugelassen wird. In Europa wird mit einer Entscheidung der Aufsichtsbehörde im ersten Quartal des nächsten Jahres gerechnet.
Lecanemab hat großen Pharmaunternehmen wie Bristol Myers Squibb und GSK Hoffnung gegeben, die sich wieder in die Neurowissenschaften einbringen, Partnerschaften mit Start-ups eingehen oder versuchen, gescheiterte Arzneimittelkandidaten wiederzubeleben.
Laut einer Studie der Universität von Nevada gibt es heute mehr klinische Studien für Alzheimer-Medikamente als je zuvor. Die Zahl der von den Arzneimittelherstellern gesponserten Studien ist im vergangenen Jahr um fast 8 Prozent gestiegen. AstraZeneca verfügt nach eigenen Angaben immer noch über eine kleine neurowissenschaftliche Gruppe mit einer Reihe von Produkten in der Erprobung, darunter eines für Alzheimer in einer frühen Studie.
Nach dem Wandel, der sich in den letzten zehn Jahren in der Onkologie vollzogen hat - die Sterblichkeitsraten sind bei vielen Krebsarten rückläufig - spekulieren Wissenschaftler, dass auch Alzheimer mit Medikamenten angegangen werden könnte, die auf bestimmte Patientengruppen zugeschnitten sind.
Lecanemab ist zwar noch lange kein perfektes Medikament, aber es ist das Ergebnis jahrzehntelanger Forschung und vieler gescheiterter Kandidaten - ein langwieriger und frustrierender Prozess von Versuch und Irrtum, der nun erste Früchte trägt. John Hardy, Professor für Neurologie am University College London, sagt, dass Wissenschaftler und Unternehmen endlich verstehen, was ein potenzielles Medikament leisten muss, um die Krankheit zu bekämpfen. "Wir tappen nicht mehr im Dunkeln", sagt er.
Die "arktische Mutation"
Der Mitbegründer von BioArctic, der Arzt und Wissenschaftler Lars Lannfelt, reiste bis ans Ende der Welt, um den Hinweis zu finden, der ihm zum Durchbruch seines Medikaments verhalf.
In den 1990er Jahren machte sich Lannfelt einen Namen in der Demenzforschung, als er bei Alzheimer-Patienten eine Mutation in dem Gen entdeckte, das ein Protein namens Amyloid beta produziert. Eine Anhäufung von Amyloid in Form von klebrigen Plaques im Gehirn wird allgemein als Ursache von Alzheimer angesehen. Allerdings stimmen nicht alle Forscher der "Amyloid-Hypothese" zu. Zahlreiche Therapien, die darauf abzielen, die Plaques im Gehirn der Patienten zu reduzieren, sind in Versuchen gescheitert, was Zweifel sät und die Spaltung vertieft.
Lannfelt machte seine Entdeckung - die er "die schwedische Mutation" taufte - nach langen und rutschigen Fahrten zu weit entfernten Gemeinden in seinem Volvo, der, wie er beklagt, keine Servolenkung hatte.
Auf der Suche nach einem Medikament zur Behandlung der Krankheit ging er sogar noch weiter: Er flog nach Umeå in Nordschweden und fuhr mit einem Mietwagen zu einer abgelegenen Gemeinde, in der Menschen lebten, die aufgrund ihrer eigenen genetischen Mutation überproportional an Alzheimer erkrankten. Bei ihnen traten "übertriebene Formen der Krankheit" auf - sie entwickelten die Symptome in einem jüngeren Alter als der Durchschnitt und erlebten einen schnelleren Verfall. Daher war es einfacher, mit Hilfe von Bluttests und Scans zu beobachten, was im Gehirn vor sich ging.
"Meine Idee war: Wenn wir die Mutationsfälle nicht verstehen, werden wir auch die häufigeren Formen nicht verstehen. Man fängt mit dem Einfachen an", sagt Lannfelt.
Lannfelt entdeckte, dass Patienten in der arktischen Gemeinschaft zwar die Symptome von Alzheimer aufwiesen, aber nicht die klebrigen Plaques im Gehirn hatten. Vielmehr hatten sie eine Anhäufung von Amyloid-Beta in einer löslichen Form, den so genannten Protofibrillen. Lannfelt kam zu der Überzeugung, dass es die Protofibrillen sind, die die Krankheit auslösen. Im Gegensatz zu den Plaques können sich die löslichen Protofibrillen im Gehirn bewegen, Neuronen verstopfen und schließlich zum Absterben der Zellen führen.
Protofibrillen, dachte er, wären auch ein sichereres Ziel für ein Medikament. Amyloid beta kommt in vielen Formen im Körper vor. Protofibrillen kommen nur im Gehirn vor. Medikamente, die auf Amyloid-Beta abzielen, könnten sich daher an unerwünschten Stellen festsetzen und schwere Nebenwirkungen verursachen.
Im Jahr 2003 wandten sich Lannfelt und seine Kollegen von BioArctic zunächst an Eisai, ein viel größeres Unternehmen mit Erfahrung in klinischen Studien mit Alzheimer-Patienten. Im Gegensatz zu vielen anderen Pharmaunternehmen zu dieser Zeit war Eisai ebenfalls entschlossen, ein Medikament gegen die Krankheit zu finden. Haruo Naito, der Vorstandsvorsitzende, leitete das Forschungslabor des Unternehmens, als Eisai seine erste Therapie für Alzheimer-Symptome entwickelte, und er blieb in Kontakt mit Patienten und ihren Familien. Alexander Scott, Executive Vice-President of Integrity, sagt, Naito verstehe den "enormen ungedeckten Bedarf" der Patienten.
Im Jahr 2007 erwarb der japanische Arzneimittelhersteller die Lizenz für Lecanemab, und 2014 schloss Eisai einen Vertrag mit Biogen zur gemeinsamen Entwicklung und Vermarktung des Medikaments.
Der heute 74-jährige Lannfelt beschäftigt sich seit 1992 mit der Alzheimer-Krankheit. Er war davon überzeugt, dass der neue Ansatz von BioArctic funktionieren würde, doch er funktionierte besser als er erwartet hatte. In der Studie verschlechterte sich der Zustand der Patienten, die das Medikament einnahmen, um 27 Prozent langsamer als bei denjenigen, die ein Placebo erhielten, gemessen an einer kognitiven und funktionellen Skala. Bei den Studienteilnehmern, die als Patienten im Frühstadium eingestuft wurden, hatte sich das Amyloid wahrscheinlich schon seit 20 bis 25 Jahren in ihrem Gehirn angesammelt. Die Scans zeigten jedoch einen deutlichen Rückgang in nur 18 Monaten.
"Ich war überrascht, dass die Wirkung so stark war", sagt Lannfelt.
Auch die Investoren waren überrascht. Die Aktien von BioArctic schossen am Tag der Veröffentlichung der ersten Ergebnisse um mehr als 240 Prozent in die Höhe. Die Analysten der schwedischen Bank Carnegie prognostizieren, dass der Umsatz im Jahr 2035 einen Höchststand von 13 Milliarden Dollar erreichen wird, was BioArctic in diesem Jahr eine Lizenzgebühr von 1,1 Milliarden Dollar einbringt. Insgesamt wird das Unternehmen Milliardenbeträge erhalten, von denen es einen Großteil in die Suche nach wirksameren Medikamenten investieren will.
Dies ist ein deutlicher Unterschied zu dem letzten Alzheimer-Medikament, das als Durchbruch gefeiert wurde. Nach einer umstrittenen beschleunigten Zulassung in den USA im Jahr 2021 weigerte sich Medicare, für das Medikament Aduhelm von Biogen und Eisai zu zahlen. Aduhelm wirkte nicht so gut, und Wissenschaftler debattierten über die Gültigkeit seiner Studien, nachdem eine gescheitert war. Der Preis für Aduhelm war ursprünglich mit 56.000 Dollar pro Jahr viel höher, wurde aber später auf 26.500 Dollar gesenkt.
Jetzt gibt es zwei Medikamente mit solideren Aussichten. Eine Ausnahme von Big Pharmas anfänglichem Exodus aus der Neurowissenschaft war das in Indianapolis ansässige Unternehmen Eli Lilly, das trotz des Scheiterns anderer Alzheimer-Medikamente am Markt blieb. Ron DeMattos, Senior Vice-President und Chief Scientific Officer of Neurobiologics bei Lilly, sagt, die Entscheidung, ein Amyloid-reduzierendes Medikament zu entwickeln, sei ein "Vertrauensvorschuss" gewesen.
Im Gegensatz zu BioArctic zielte Lilly auf die feste Form von Amyloid beta, die Plaques. Das Molekül erwies sich als erfolgreich: Donanemab verlangsamte das Fortschreiten der Krankheit bei 1.182 Patienten um 35 Prozent - eine kleinere Gruppe als bei den Lecanemab-Studien. Die Studie zeigte auch Nebenwirkungen wie Hirnschwellungen und Blutungen. Die vollständigen Studienergebnisse sind jedoch noch nicht veröffentlicht worden.
"Ich glaube, dass das Feld jetzt über dieses ganze Hin und Her, Amyloid-Hypothese oder nicht Amyloid-Hypothese, hinausgehen kann", sagt DeMattos. "Die eigentliche Frage lautet: Wie können wir den Nutzen für die Patienten weiter steigern? Wie können wir diesen Erfolgskurs fortsetzen, um die Margen zu verbessern, damit es den Patienten im Laufe der Zeit besser geht?"
Hardy, Professor für Neurologie am UCL, sagt, das eigentliche Problem mit den bisherigen Medikamenten, die auf Beta-Amyloid abzielten, sei, dass sie nicht genug davon entfernten. "Für mich sehen die beiden [neuen] Medikamente ziemlich ähnlich aus, beide entfernen Amyloid, und beide haben ähnliche klinische Auswirkungen", sagt er.
Rob Howard, Professor für Alterspsychiatrie an derselben Einrichtung, ist jedoch anderer Meinung. Er räumt ein, dass Amyloid-Beta mit Alzheimer in Verbindung steht, bezweifelt aber, dass es das Fortschreiten der Krankheit fördert. Er ist der Ansicht, dass die Korrelation zwischen der Menge an abgebautem Amyloid und dem klinischen Nutzen für die Patienten in der Lecanemab-Studie gering war.
"Goldenes Zeitalter" der Alzheimer-Forschung ins Sicht?
Seit den erfolgreichen Studienergebnissen von Lecanemab und Donanemab ist das Interesse großer Pharmakonzerne, die neurowissenschaftliche Biotech-Unternehmen erwerben wollen, deutlich gestiegen, sagt Philip Scheltens, der den mit 260 Millionen Euro ausgestatteten LSP Dementia Fund leitet. "Wir sind jetzt in einer guten Position, weil Big Pharma plötzlich wieder Interesse zeigt", sagt er.
Obwohl es ähnlich viele Patienten gibt, ist Demenz immer noch weit weniger erforscht als Krebs, was zum Teil daran liegt, dass sie weniger Mittel erhält, sagt Scheltens. In der Online-Datenbank PubMed wurden etwa 4,8 Millionen Artikel über Krebs veröffentlicht, im Vergleich zu 264.000 über Demenz.
Osswald ist sich bewusst, dass Big Pharma jetzt auf das kleine Stockholmer Unternehmen aufmerksam wird, und hält sich deshalb bedeckt, was BioArctic sonst noch für die Alzheimer-Krankheit erforscht. Aber das Unternehmen ist inspiriert von einem Wandel in der Onkologie. Anders Martin-Löf, Chief Financial Officer, sagt, dass die Onkologie das "große Ding" der letzten 10 Jahre war, mit gezielteren Medikamenten, die oft für eine bessere Wirkung kombiniert werden.
"Wir stehen jetzt am Anfang der Neurologie. Und ich glaube, dass wir vor einer goldenen Ära stehen, die bald beginnt", sagt er.
Auch wenn die Amyloidbildung das erste Anzeichen von Alzheimer ist, gibt es noch andere Ziele, die angegangen werden müssen, wie die Tau-Proteine, die sich im Gehirn der Patienten ansammeln. Eisai testet bereits Lecanemab in Kombination mit einem Medikament, das gegen Tau wirkt.
In dem Maße, wie die Tests genauer werden und wir mehr über die Vorgänge im Inneren des Einzelnen verstehen, können Medikamente gezielt auf bestimmte Gruppen ausgerichtet werden, wie bei Krebs, wo viele Tumore sequenziert werden, um herauszufinden, welche Mutationen sie antreiben, und dann spezifische Medikamente verschrieben werden. Einige glauben, dass Alzheimer am Ende vielleicht nicht einmal eine einzelne Krankheit ist.
BioArctic sucht auch nach Möglichkeiten, Beta-Amyloid effektiver zu bekämpfen. Sein "Moonshot"-Projekt ist ein "Gehirntransporter", mit dem mehr Medikamente ins Gehirn gelangen sollen. Derzeit kann nur etwa 1 Prozent eines Medikaments die strenge Blut-Hirn-Schranke überwinden, so dass die Patienten hohe Dosen erhalten müssen und Nebenwirkungen riskieren. Das Unternehmen hofft, durch die Entführung des Systems, das Eisen ins Gehirn transportiert, Zugang zu den 600 km langen Blutgefäßen im Inneren des Organs zu erhalten.
Zoe Karamanoli, Analystin bei RBC Capital Markets, die sich mit BioArctic befasst, sagt, dass der Gehirntransporter "ein enormes Potenzial" habe, aber in diesem Stadium noch sehr riskant sei. Sie sagt, dass BioArctics Geldsegen aus den Lecanemab-Lizenzgebühren dem Unternehmen helfen wird - aber es ist nicht genug, um einen zweiten Erfolg zu garantieren. "Es hilft ihnen auf jeden Fall, etwas zu haben, das funktioniert hat und in einem so schwierigen Bereich zugelassen ist. Aber man sollte nicht davon ausgehen, dass alles funktionieren wird", warnt sie.
Lecanemab befindet sich bereits in Phase-3-Studien für eine Bevölkerungsgruppe mit weniger Amyloid im Gehirn, die noch keine Symptome aufweist.
Andere Unternehmen streben ebenfalls einen früheren Zeitpunkt an. Letzte Woche erhielt AC Immune von der FDA die Zulassung für einen "Alzheimer-Impfstoff", von dem man hofft, dass er das Immunsystem dazu anregt, die Ablagerung von Proteinen selbst zu bekämpfen.
Ein glücklicher Zufall will es, dass schwedische Wissenschaftler im Jahr 2020 einen Bluttest entwickelt haben, mit dem die frühen Stadien der Ablagerungen im Gehirn erkannt werden können, noch bevor eine Behandlung in Frage kommt. Der Test kann die Krankheit fünf bis zehn Jahre vor einer deutlichen Beeinträchtigung der Patienten erkennen.
Einige Experten sind der Meinung, dass die derzeitigen Medikamente zu schwerwiegende Nebenwirkungen haben, um asymptomatische Menschen zu behandeln, während andere hoffen, dass es weniger Nebenwirkungen geben könnte, wenn weniger Amyloid an den Blutgefäßen haftet.
Scott von Eisai, dessen eigene Eltern an Alzheimer starben, verglich die Einnahme von Medikamenten zur Vorbeugung der Krankheit mit den "ziemlich radikalen Eingriffen", die manche bereit sind, vorzunehmen, um das Krebsrisiko zu verringern. "Die Leute lassen sich eine doppelte Mastektomie durchführen, wenn sie eine familiäre Vorbelastung haben, wie Angelina Jolie uns gezeigt hat", sagt er.
Wenn Lecanemab präventiv eingesetzt wird, könnte BioArctic weitere Milliarden verdienen. Osswald hat Ambitionen, BioArctic zu einem eigenständigen Pharmaunternehmen auszubauen, das große Studien durchführt und seine eigenen Medikamente weltweit vertreibt.
Aber sie will nicht, dass es das nächste AstraZeneca wird, das sich ihrer Meinung nach in der Bürokratie verzetteln könnte. BioArctic beschäftigt gerade einmal 85 Mitarbeiter in einem Büro und in Labors, die sich über ein paar Stockwerke in Stockholm verteilen.
Sie hat auch keine Angst vor der Konkurrenz, wenn andere große Pharmaunternehmen wieder in das Rennen um bessere Alzheimer-Behandlungen einsteigen. "Wir haben keine Angst vor Wettbewerb. Ich denke, das ist hilfreich für die Patienten", sagt sie. "Der Markt ist riesig."
1 note
·
View note
Photo

News Alert: Alzheimer’s drug lecanemab receives accelerated approval from the @FDA : @CNN The US Food and Drug Administration granted accelerated approval Friday for the Alzheimer’s disease drug lecanemab, one of the first experimental dementia drugs to appear to slow the progression of cognitive decline. #news #medicine #health #brain #longevity #Alzheimer #health #lecanemab #fdaapproval #IMRAN (at imran.tv) https://www.instagram.com/p/CnFm9AQpPtj/?igshid=NGJjMDIxMWI=
0 notes
Text
Lecanemab, il farmaco che dà nuove speranze contro l'Alzheimer, rallentandone i progressi
Allo studio del farmaco - sviluppato da una casa farmaceutica giapponese e da una americana - hanno partecipato 1.800 persone che vivono le prime fasi della malattia che "ruba la memoria". Il farmaco ha ritardato il peggioramento dei pazienti di circa cinque mesi
0 notes
Link

Im Jahr 1906 berichtete Alois Alzheimer erstmals über "einen eigentümlichen schweren Krankheitsprozess der Großhirnrinde". Es handelte sich um eine 50-jährige Frau, die unter Gedächtnisverlust, Wahnvorstellungen, Halluzinationen, Aggression und Verwirrung litt, die sich bis zu ihrem frühen Tod fünf Jahre später verschlimmerten. Bei der Autopsie stellte Alzheimer auffällige Plaques in ihrem Gehirn fest. Diese Plaques - Klumpen des Amyloid-beta-Proteins - werden immer noch als Ursache der Alzheimer-Krankheit angesehen.
Die Plaque-Theorie erklärt allerdings nicht, warum viele Personen (auch alte Menschen) Plaques in ihrem Gehirn haben, ohne dass neurologische Symptome wie Gedächtnisverlust auftreten. Außerdem waren klinische Versuche mit Arzneimitteln, die diese Ablagerungen reduzieren, bisher erfolglos - mit einer kürzlichen Ausnahme, aber dazu später mehr.
Wenn sich Amyloid-beta-Protein in Form von Plaques (unlöslichen Klumpen) ansammelt, wird die ursprüngliche lösliche Form des Proteins, die wichtige Funktionen im Gehirn erfüllt, verbraucht und geht verloren. Einige Studien haben gezeigt, dass geringere Mengen an löslichem Amyloid-beta - Amyloid-beta 42 genannt - zu einem schlechteren klinischen Ergebnis bei den Patienten führen.
In einer kürzlich im Journal of Alzheimer's Disease veröffentlichten Studie wurde untersucht, ob die Menge der Plaques im Gehirn oder die Menge des verbleibenden Amyloid-beta 42 für das Fortschreiten der Alzheimer-Krankheit wichtiger ist. Um diese Frage zu beantworten, sahen sich Wissenschaftler die Daten einer Gruppe von Menschen an, die eine seltene vererbte Genmutation aufweisen, die sie einem hohen Risiko aussetzt, an Alzheimer zu erkranken. Die Teilnehmer stammten aus der Kohortenstudie des Dominant Inherited Alzheimer Network.
Die Forscher fanden heraus, dass der Abbau von Amyloid-beta 42 (die funktionelle Version von Amyloid-beta) schädlicher ist als die Menge der Plaques (die unlöslichen Klumpen von Amyloid-beta). Die Teilnehmer wurden im Durchschnitt drei Jahre lang beobachtet. Es zeigte sich, dass diejenigen mit hohen Amyloid-beta-42-Werten im Liquor (der Flüssigkeit, die das Gehirn und das Rückenmark umgibt) geschützt waren und ihre kognitiven Fähigkeiten während des Studienzeitraums erhalten blieben. Dies deckt sich mit vielen Studien, in denen wichtige Funktionen von Amyloid-beta 42 für Gedächtnis und Kognition nachgewiesen wurden.
Der Befund ist auch deshalb von Bedeutung, weil Menschen mit der genetischen Mutation untersucht wurden, die an Alzheimer erkranken, eine Gruppe, die als der stärkste Beweis für die Idee gilt, dass Amyloid-beta-Plaques schädlich sind. Doch selbst in dieser Gruppe blieben die Personen mit höheren Amyloid-beta-Spiegeln im Liquor (CSF) kognitiv normal, unabhängig von der Menge der Plaques in ihrem Gehirn.
Erwähnenswert ist auch, dass bei einigen seltenen, vererbten Formen der Alzheimer-Krankheit - z. B. bei Trägern der so genannten Osaka-Genmutation oder der Arktis-Mutation - Menschen eine Demenz entwickeln können, die niedrige Amyloid-beta-42-Spiegel und keine nachweisbaren Plaques aufweisen. Dies deutet darauf hin, dass nicht die Plaques, sondern die niedrigen Amyloid-beta-42-Konzentrationen die Ursache für die Demenz sind.
Lecanemab - die große Ausnahme
Wie werden sich diese Erkenntnisse auf die Entwicklung von Arzneimitteln und die klinischen Studien zur Alzheimer-Krankheit auswirken? Bis zur jüngsten Studie mit Lecanemab, einem Antikörperpräparat, das die Plaques reduziert, sind alle Versuche mit Arzneimitteln gegen die Alzheimer-Krankheit gescheitert.
Einige Medikamente zielten darauf ab, die Amyloid-beta-42-Konzentration zu verringern, weil man davon ausging, dass die Patienten weniger Plaques bilden, wenn die Konzentration des normalen Proteins verringert wird. Leider haben diese Medikamente den Zustand der Patienten oft verschlechtert.
Kürzlich wurde berichtet, dass Lecanemab eine geringe, aber signifikante Wirkung bei der Verringerung des kognitiven Verfalls hat. Nach früheren Studien erhöht dieses Medikament die Amyloid-beta 42-Konzentration im Liquor. Dies steht wiederum im Einklang mit der Hypothese, dass die Erhöhung des normalen Amyloid-Proteins von Vorteil sein kann.
Die Autoren der oben genannten Studie halten es für wichtig, dass sich künftige Studien auf die Amyloid-beta-42-Konzentration konzentrieren und prüfen, ob es von Vorteil ist, die Konzentration zu erhöhen und wieder auf normale Werte zu bringen, anstatt sie gezielt zu beseitigen.
Dieser Ansatz des aktiven Proteinersatzes könnte ein neuer Weg zur Behandlung der Alzheimer-Krankheit sein. Bisher war es so, dass sich die an Alzheimer erkrankten Patienten bestenfalls ein wenig Zeit mit Medikamenten wie Memantin oder Donepezil kaufen konnten. Mit den neuen Ansätzen besteht aber Grund zu vorsichtigem Optimismus, dass die Erkrankung irgendwann sogar heilbar sein wird.
0 notes
Text
Dementia growing.Till potus?
more anxious, depressed, irritated, hobbies change, falls and shuffling are lesser known signs of #Alzheimer
#lecanemab newest treatment
citizens with #dementia like #Biden aren't leaders of the free world & don't have the president's responsibilities
0 notes
Text
Alzheimer’s Drug Shows Promise in Early Results of Study
Alzheimer’s Drug Shows Promise in Early Results of Study
Shares of Biogen and other drugmakers researching Alzheimer’s disease soared early Wednesday after Japan’s Eisai Co. said its potential treatment appeared to slow the fatal disease’s progress in a late-stage study.
Eisai announced results late Tuesday from a global study of nearly 1,800 people with early-stage Alzheimer’s.
The drugmaker said early results showed that its treatment, lecanemab,…

View On WordPress
0 notes